앞선 글에서 Ramachandran Plot을 설명하면서 폴리펩타이드에서 φ(Phi)와 ψ(Psi)이 무엇인지를 설명했었다. 그런데 단순하게 언급하고 넘어간 것 만으로는 이해하기 힘든 점들이 꽤 있을 것 같아서 추가적인 글을 작성하였다. 우선 이전 글에서 적었던 글을 간단하게 요약하고 넘어가자.

- φ(Phi): 알파 탄소와 알파 탄소에 결합된 질소(아미노기에서 유래) 사이의 회전각
- ψ(Psi): 알파 탄소와 알파 탄소에 결합된 탄소(카보닐기에서 유래) 사이의 회전각
- 각도는 시계 방향으로 회전할 때 양수, 반시계 방향으로 회전할 때 음수로 나타낸다
- 가능한 회전각의 범위는 -180도에서 180도 범위이다.
정의는 단순하다. 그런데 알파 탄소에 결합한 질소와 탄소 그 자체는 회전해도 크게 달라지는 게 없는데 무엇을 기준으로 회전각을 측정하라는 걸까? 마치 두 공을 막대기 하나로 연결했을 때, 한쪽 공을 아무리 막대기를 기준으로 회전시켜도 전과 후에 큰 차이가 없는 것과 같다.
방법은 있다. 해당 질소와 탄소에 결합한 다른 원자들의 회전 정도를 측정하면 된다. 펩타이드 결합 덕분에 같은 평면 상에서 6개의 원자가 함께 회전한다는 점은 앞서 언급한 바 있다. 이를 활용하면 회전 여부 및 정도를 측정할 수 있다.
그러면 먼저 φ(Phi)를 측정하는 법부터 알아보자. φ(Phi)를 측정할 줄 알면 ψ(Psi)를 측정하는 것은 자연스럽게 따라온다.
우선 머릿속에 위에 나와있는 폴리펩타이드의 3차원 구조를 한번 상상해보자. 우선 펩타이드 결합의 중심에 있는 알파 탄소는 각각 질소(아미노기), 탄소(카보닐기), 수소, Side chain 총 4개 그룹에 각각 단일 결합으로 연결되어 있기 때문에 사면체 구조를 띨 것이다. 알파 탄소는 사면체의 중심에 위치하며, 각 그룹은 사면체의 꼭짓점에 위치할 것이다. 사면체는 우리가 원할 경우 같은 평면 상에 있는 세 꼭짓점을 동일하게 바닥에 두고, 나머지 하나를 위에다가 놓을 수 있다. 이를 위의 경우에도 적용시킬 수 있다.
우선 φ(Phi)를 측정하기 위해서는 N(amide)-C(alpha) 결합을 일직선 상에 놓아야 한다. 기준이 되기 때문이다. 쉽게 생각하면 알파 탄소를 바라볼 때, 질소를 알파 탄소 바로 뒤에 놓는다고 생각해보자. 그러면 알파 탄소에 결합되어 있는 나머지 탄소, 수소, Side chain은 같은 평면 상에서 위치하게 된다. 아래의 그림을 통해 한번 머릿속으로 이미지를 떠올려보자.
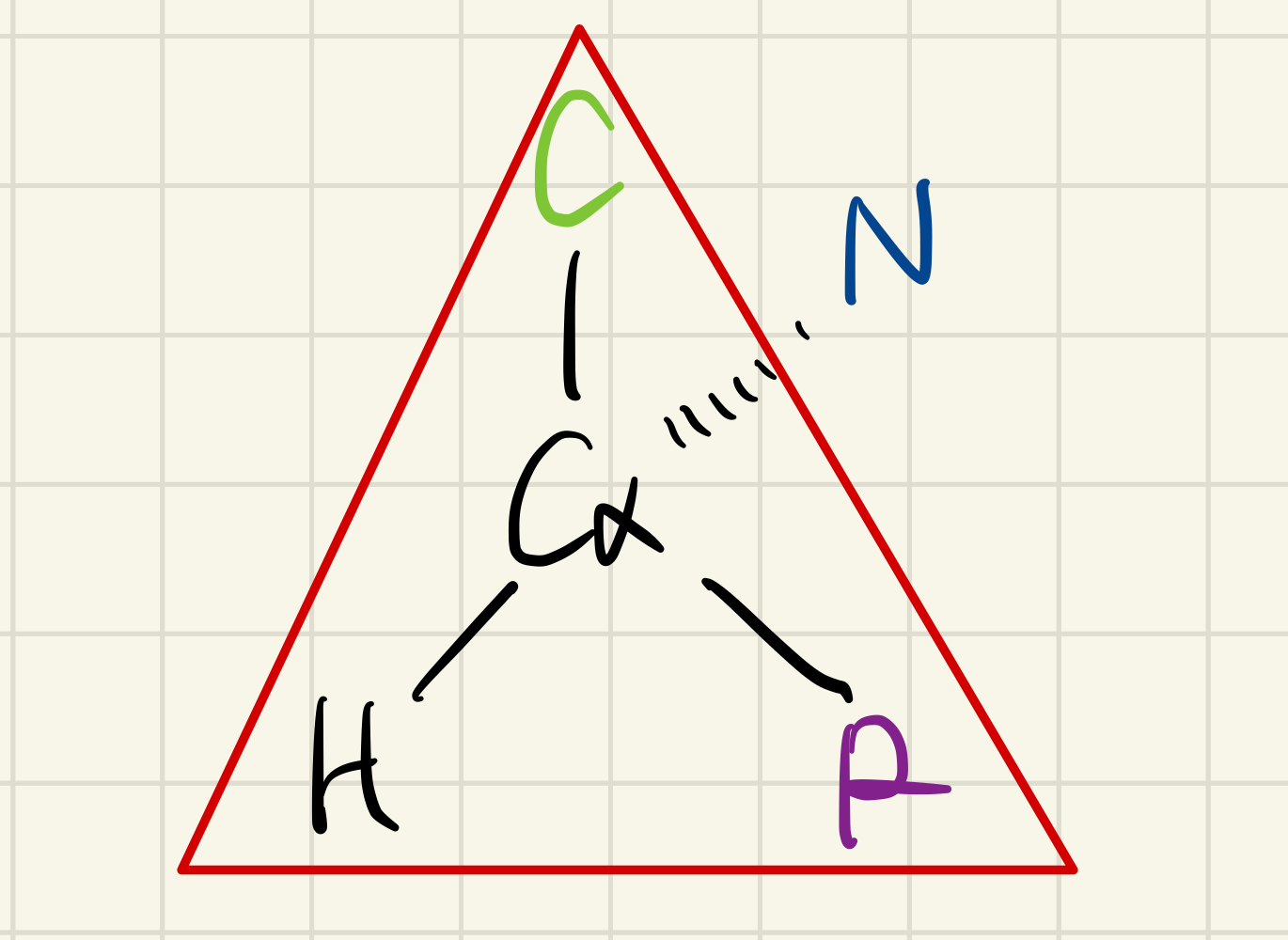
이 그림에서 탄소, 수소, R(Side chain)은 모두 같은 평면 상에 존재한다. 질소는 점선을 통해 보이는 것처럼 표시되었지만, 실제로는 알파 탄소에 가려져서 보이지 않는 위치에 있다. 즉 질소-알파 탄소 결합을 알파 탄소 뒤에서 바로 바라보고 있는 것이다.
지금 위 그림에서 녹색으로 표시된 탄소가 기준점이 된다. 알파 탄소에 가려진 질소는 펩타이드 결합을 통해 다른 아미노산의 카보닐기 탄소와 연결되어 있다. 알파 탄소에 직접 연결된 탄소와 가려진 질소에 연결된 탄소 사이의 각도가 φ(Phi)가 된다. 그럼 예를 들어서 맨 처음 소개된 그림에 나와있는 상태처럼 원자들이 배치되어있다고 생각해보자.
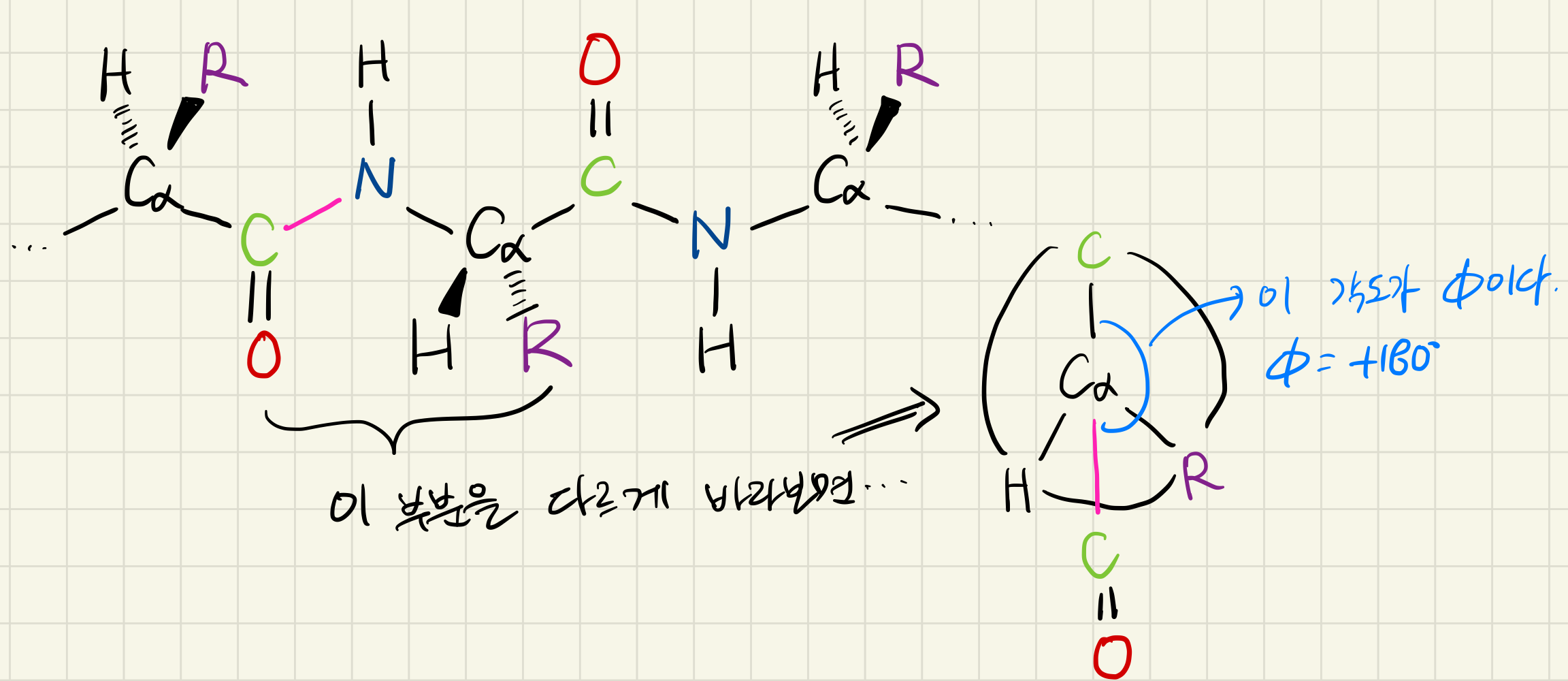
분홍색으로 표시된 펩타이드 결합은 앞서 언급한 시선에서 바라봤을 때 오른쪽처럼 보일 것이다. 따라서 두 탄소 사이의 각도를 측정하면 +180도가 된다. (-180도와 180도로 모두 해석할 수 있으나, 일반적으로는 양수로 표현한다)
그럼 반대로 ψ(Psi)를 측정해보자. ψ(Psi)는 반대로 알파 탄소 사면체에서 카보닐기의 탄소를 알파 탄소 뒤에 놓고 생각하면 된다. 마치 아래 그림처럼 말이다. 달라진 점은 크게 두가지이다. 아까와는 달리 질소, 수소, Side chain이 같은 평면에 놓여있다는 점, 그리고 수소와 Side chain의 위치가 서로 달라진 것이다. 이때 수소와 Side chain의 위치가 달라지는 이유는 같은 사면체를 서로 다른 시선에서 보았기 때문이다. 실수로 바꿔서 그리면 아예 다른 구조가 되니 헷갈리면 안된다!

φ(Phi)를 측정할 때 알파 탄소에 직접 결합한 탄소, 숨겨진 질소에 펩타이드 결합으로 연결된 탄소 사이의 각을 측정했던 것을 반대로 적용하면 ψ(Psi)를 측정할 수 있다. 알파 탄소에 직접 결합한 질소,숨겨진 탄소에 펩타이드 결합으로 연결된 질소 사이의 각을 측정한 것이 바로 ψ(Psi)이다.
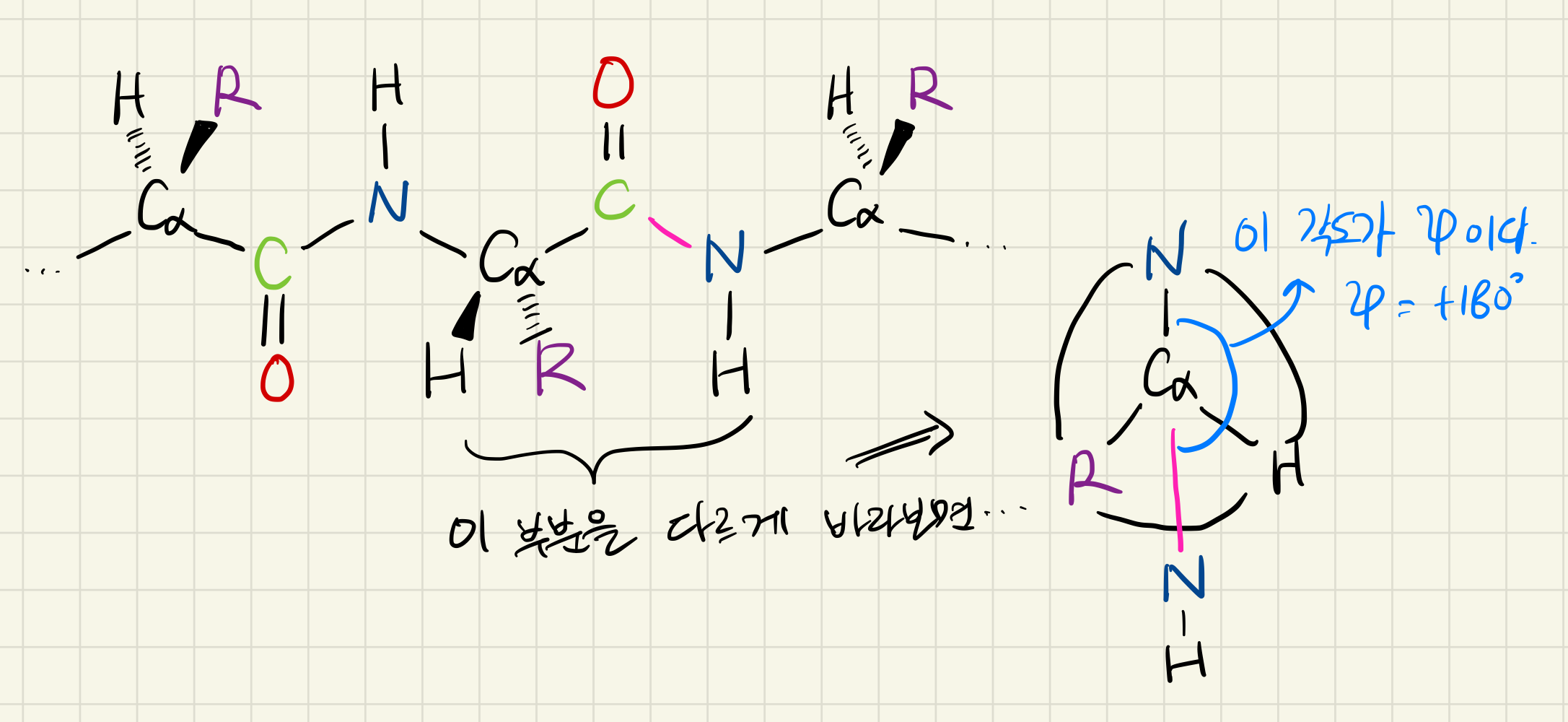
마찬가지로 분홍색으로 표시된 펩타이드 결합이 위에서 언급한 시선으로 바라보면 아래와 같이 보일 것이다. 따라서 질소들 사이의 각도를 측정하면 이 경우는 +180도가 된다. 왜 양수와 음수 중 양수로만 표현하는지 이유는 위와 같다.
즉, 위와 같이 폴리펩타이드 서열에서 Back bone이라고도 불리는 알파 탄소, 탄소, 질소 사이의 결합이 평평하게 나타나기 위해서는 φ(Phi)와 ψ(Psi)가 각각 +180도여야 함을 알 수 있다. 물론, Ramachandran Plot이 알려주듯이 이 조합은 자연에서 일반적으로 나타나지 않는 조합이다. 그러면 좀 더 다양한 각도의 경우 원자들의 배치가 어떻게 이뤄지는지 그림을 통해 알아보도록 하자. 역시나 분홍색으로 표시된 결합은 펩타이드 결합이다.

즉 요약하면 다음과 같다.
- 측정하고 싶은 각에 해당하는 결합(예: N(amide)-C(alpha) 결합)을 알파 탄소가 위로 오게 바라본다. 즉, 다른 원자가 보이지 않는 방향에서 결합을 바라본다
- φ(Phi)의 경우는 알파 탄소에 직접 결합한 탄소를, ψ(Psi)는 알파 탄소에 직접 결합한 질소를 기준점(0도)로 삼는다.
- 펩타이드 결합을 통해 연결된 반대 편의 탄소 또는 질소와 기준점 사이에 이루는 각을 측정한다. (만약 두 탄소 또는 두 질소가 겹쳐서 보이면 그때의 각은 0도가 된다)
'생화학I' 카테고리의 다른 글
| [생화학I] 6. 단백질의 2차 구조 (2) 베타 병풍, Turn, Loop (0) | 2023.07.07 |
|---|---|
| [생화학I] 5. 단백질의 2차 구조 (1) 알파 나선 (0) | 2023.07.06 |
| [생화학I] 4. 펩타이드 결합과 Ramachandran Plot (0) | 2023.07.03 |
| [생화학I] 3. 특이한 아미노산 3가지 (프롤린, 시스테인, 히스티딘) (0) | 2023.06.30 |
| [생화학I] 2. 아미노산의 구성과 특징 (0) | 2023.06.29 |



